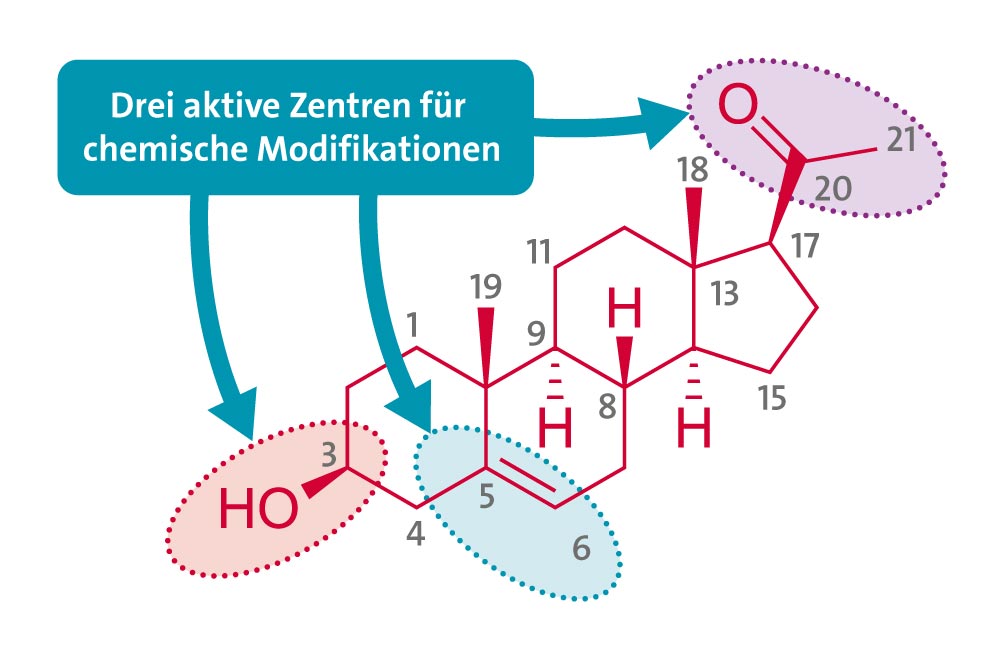
Strukturelle Veränderungen von Pregnenolon wurden durch die Einführung heterocyclischer Reste an der C-17-Position durch Begrenzung der Acylgruppe vorgenommen.
Neue heterocyclische Pregnenolon-Analoga wurden unter Verwendung der Friedlander- und Claisen-Schmidt-Reaktion synthetisiert und die synthetisierten Verbindungen auf ihre osteogene Aktivität untersucht.
Unter den synthetisierten Derivaten zeigten vier Verbindungen eine signifikant erhöhte ALP-Aktivität. Unter allen vier Wirkstoffen hat die neue Verbindung 3a eine signifikante Mineralisierung der Knochenmatrix und mRNA-Expressionen von osteogenen Markergenen, BMP2, RUNX-2 und OCN bei 1pM-Konzentration gezeigt.